一、目的
了解并掌握氨基酸紙層析的原理和方法。
二、原理
以濾紙為支持物的層析法,稱為紙層析法。紙層析所用展層劑大多由水和有機溶劑組成。展層時,水為靜止相,他與濾紙纖維親和力強;有機溶劑為流動相,它與濾紙纖維親和力弱。有機溶劑在濾紙上又下向上移動的,稱為上行法;有上向下移動的,稱為下行法。
將樣品在濾紙上確定的原點處展層,由于樣品中各種氨基酸在兩相中不斷進行分配,且他們的分離系數各不相同,所以不同的氨基酸隨流動相移動的速率也不相同,于是各種氨基酸在濾紙上就相互分離出來,形成距原點不等的層析點。在一定條件下(室溫、展層劑的組成、濾紙的質量、PH值等不變),不同的氨基酸有固定的移動速率(Rf值)
Rf=原點到層析點中心的距離/原點到溶劑前沿的距離
用混合氨基酸做樣品時,如果只用一種溶劑展層,由于某些氨基酸的移動速率相同或相近,就不能將它們分開,為此,當用一種溶劑展層后,可將濾紙旋轉90度,以**次所的層析點為原點,在用另一溶劑展層,從而達到分離的目的。這種方法稱為雙向層析法。
本試驗主要介紹的是單向層析法。其中混合氨基酸有精氨酸、酪氨酸、苯丙氨酸組成。
三、實驗儀器 1、 新華濾紙 2、 層析缸 3、 細線 4、 點樣管 5、 橡皮筋 6、 電吹風 7、 噴霧器
四、實驗試劑
1、混合氨基酸溶液(甘氨酸,苯丙氨酸),甘氨酸溶液,苯丙氨酸溶液 2、展層劑:正丁醇:12%氨水:95%乙醇:蒸餾水=13:3:3:1(v:v) 3、0.5%茚三酮—無水丙酮溶液:0.5g茚三酮溶于100ml無水丙酮,貯于棕色瓶中
五、試驗步驟
1、取濾紙剪成20×10厘米的濾紙條一張,在一端打孔,系一根細線,在另一端2~3cm處用鉛筆畫一橫線,中間畫一圓點(原點)。
2、取毛細管一支(回收),吸取氨基酸混合液,在原點處點樣,樣點直徑不宜超過5mm,每點一次用吹風機吹干,點2~3次為佳。
3、點樣后將濾紙放入層析缸中展層,注意點樣線要高于層析液面,濾紙不要貼在層析缸璧上,當展層**另一端1~2cm處時,停止展層(大約2~3小時)。 4、取出濾紙,用鉛筆記下溶劑前沿,然后用熱風吹干(或烘箱60℃)烘干。 5、均勻噴上茚三酮—無水丙酮液,注意使溶液不倒流,不間斷。 6、用吹風機吹干,觀察層析點,確定其幾何中心。
7、量取數值,計算各自的Rf值,與表中標準氨基酸Rf值比較,確定樣品氨基酸種類。(書上圖譜橫著看)
六、實驗結果
1.標準氨基酸單向上行層析法 定性、定量測定:
將樣品在濾紙上確定的原點處展層,由于樣品中各種氨基酸在兩相中不斷進行分配,且他們的分離系數各不相同,所以不同的氨基酸隨流動相移動的速率也不相同,于是各種氨基酸在濾紙上就相互分離出來,形成距原點不等的層析點。
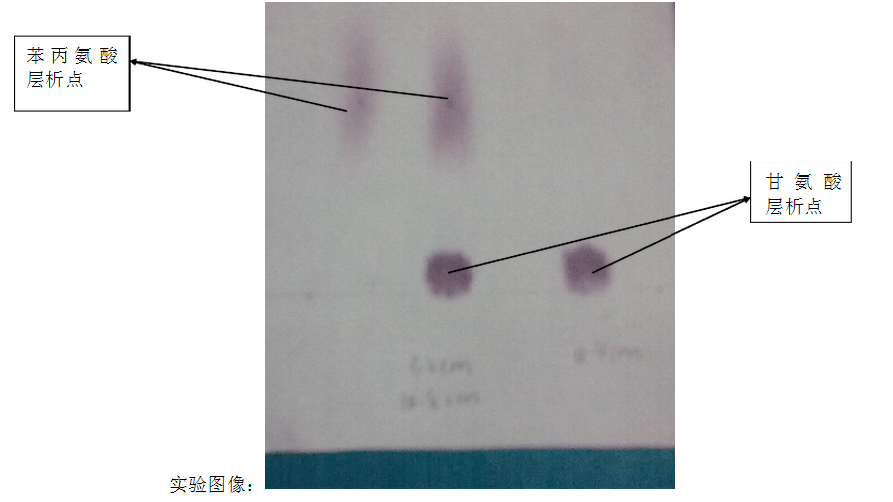
甘氨酸層析點中心到原點的距離:0.4cm 苯丙氨酸層析點中心到原點的距離:3.2cm 原點到溶劑前沿的距離:10.8cm
在一定條件下(室溫、展層劑的組成、濾紙的質量、PH值等不變),不同的氨基酸有固定的移動速率(Rf值)
Rf=原點到層析點中心的距離/原點到溶劑前沿的距離 Rf(甘氨酸)= 0.4cm/10.8cm =0.037 Rf(苯丙氨酸)= 3.2cm/10.8cm =0.296
七、實驗分析
由于樣品中各種氨基酸在兩相中不斷進行分配,且他們的分離系數各不相同,所以不同的氨基酸隨流動相移動的速率也不相同,于是各種氨基酸在濾紙上就相互分離出來,形成距原點不等的層析點。
注意事項:
1. 在原點處點樣,樣點直徑不宜超過5mm,每點一次用吹風機吹干,點2~3次為佳。防止擴散面積過大,使展層效果不佳或直接影響實驗結果。否則分離不好,并且樣品用量大,會造成“拖尾巴”的現象, 防止氨基酸斑點重疊。
2. 注意點樣線要高于層析液面。防止點樣氨基酸溶解于層析液中。濾紙不要貼在層析缸璧上。防止濾紙左右兩端展層速度過快,影響實驗結果。
3. 均勻噴上茚三酮—無水丙酮液,注意使溶液不倒流,不間斷。
4.取濾紙前,要將手洗凈,這是因為手上的汗漬會污染濾紙。并盡可能少接觸濾紙。在整個操作過程中,手只能接觸濾紙邊緣,否則手指上的氨基酸會造成濾紙上眾多斑點.要將濾紙平放在潔凈的濾紙上,不可放在試驗臺上,以防止污染。
5.展層結束后,切勿忘記用鉛筆描出溶劑前沿。 6.在點樣時,不要將毛細管插錯了試劑瓶。
7.展層劑接觸濾紙時一定要均勻、保持前沿線與濾紙平行。 8.風溫度不宜過高,否則斑點變黃。 9.影響Rf值的因素有:
①物質本身的化學結構; ②展層所用溶劑系統; ③展層劑pH值; ④展層時的溫度; ⑤展層所用濾紙; #p#分頁標題#e#
⑥展層的方向(橫向,上行或下行)。
